Besserung bei Muskeldystrophien durch Verlangsamung des Muskels
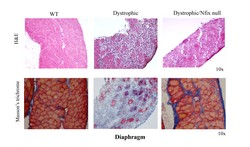
Patienten mit MD wie beispielsweise der Duchenne-Muskeldystrophie leiden an Dystrophie oder Abbau von Skelettmuskeln, wodurch die Bewegung beeinträchtigt wird. Im schlimmsten Fall sind Atmung und Herzfunktion betroffen, was zur Abhängigkeit vom Rollstuhl, Atemversagen und vorzeitigem Tod führt. Es gibt noch keine therapeutische Lösung für diese schwerwiegenden genetischen Störungen, und Versuche, die auf der Induktion des Muskelaufbaus basieren, um dem fortschreitenden Abbau entgegenzuwirken, hatten nur wenig oder vorübergehenden Erfolg. Ganz neuer Blick auf eine Therapie für MD Das Projekt RegeneratioNfix hat einen radikalen, bahnbrechenden Ansatz zur Verlangsamung von MD unternommen. In früheren Untersuchungen zeigte das Team, dass der Transkriptionsfaktor Nuclear Factor IX (Nfix) den Wechsel von der embryonalen zur fetalen Muskelbildung antreibt - von langsamen zu schnellen Zuckungen und reiferen Muskelfasern. Prof. Graziella Messina, Forschungsleiterin des Projekts, skizziert den Vorstoß insgesamt und den Grundgedanken des Projekts: „Dieses Projekt zielte darauf ab, einen begrifflich andersartigen Machbarkeitsnachweis einzuführen, um die Muskulatur bei dystrophischen Patienten zu schützen und zu erhalten.“ Obwohl dieses Konzept bereits durch Nfix-Silencing demonstriert wurde, deuteten alle Beweise darauf hin, dass andere mögliche pharmakologischen Ansätze zur Verringerung der Muskelregeneration und zur Förderung eines langsameren Muskelzuckens gleichermaßen wirksam sein könnten. Bei der Bewertung dieser Forschungsergebnisse beschreibt Prof. Messina: „Wir haben vorgeschlagen, dass ein langsamer zuckender und sich regenerierender Muskel der dystrophischen Muskeldegeneration entgehen könnte. Doch wenn Muskeln gezwungen sind, sich zu regenerieren, kann dies paradoxerweise den Phänotyp verschärfen.“ Testen der Effekte von Nfix Die Forscher kreuzten verschiedene MD-Tiermodelle mit Mäusen ohne Nfix. Die Ergebnisse zeigten eine eindrucksvolle Verbesserung der beobachtbaren körperlichen (phänotypischen) und funktionellen Symptome im Zusammenhang mit dystrophischen Muskeln bei bis zu sechs Monate alten Tieren. „Wichtig ist, dass diese Besserung auch im mdx-Duchenne-Mausmodell beobachtet wurde, was die allgemeine Gültigkeit dieses Ansatzes zeigt“, betont Prof. Messina. Ein Mangel an Nfix führte bei akuten Verletzungen zu einer verzögerten und langsamen Muskelregeneration und löste die Umwandlung der Muskulatur hin zu einem oxidativen Metabolismus aus, wie in Cell Reports beschrieben wurde. Was den Schutz des dystrophischen Muskels vor weiterer Degeneration angeht, so führt die Abwesenheit von Nfix zu einem allgemeinen Wechsel hin zu einer langsam zuckenden Kontraktion und einer reduzierten Muskelregeneration, die im Lauf der Zeit besser vor Muskelabbau schützen kann. Diese Ergebnisse werden jetzt in Nature Communications abgedruckt. Nfix-Modulation für zukünftige MD-Therapeutika Das RegeneratioNfix-Team arbeitet auch über das Projektende hinaus an Nfix und seiner therapeutischen Anwendung bei MD. Der Schwerpunkt liegt auf der Rolle von Nfix bei Makrophagen, den wichtigsten Akteuren der Gewebeentzündung. Während der Projektlaufzeit identifizierten und charakterisierten die Forscher Teile des Signalwegs, der Nfix vorgelagert ist. Prof. Messina glaubt, dass dieser Forschungsverlauf zu möglichen pharmazeutischen Interventionen führen wird, um die Nfix-Produktion zu hemmen. „Im Einklang damit wird ein kranheitsrelevanter Weg zur Hemmung von Nfix oder seiner Funktion das zukünftige Forschungsthema meines Labors darstellen.“ Parallel dazu entwickeln die Forscher spezifischere Wege zur Hemmung von Nfix, unter Verwendung von molekularem Design auf der Grundlage der kristallinen Struktur des Transkriptionsfaktors. „Die beiden Ansätze werden ein translationales Ergebnis des Projekts RegeneratioNfix darstellen, das als eine Studie in der Grundlagenforschung begann und dessen Ergebnisse zu einer echten Chance auf die Entwicklung einer potenziellen Therapie für MD-Patienten werden könnten“, stellt Prof. Messina die Errungenschaften des Projekts zusammenfassend dar.
Schlüsselbegriffe
Muskel, Muskeldystrophie, Therapie, RegeneratioNfix, Nfix