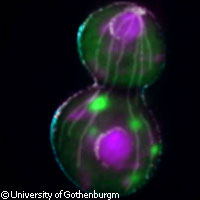
Forscher lösen Rätsel um Verjüngung alter Zellen
Forscher haben entdeckt, wie aus alten, verbrauchten Mutterzellen gesunde neue Tochterzellen entstehen, ein Prozess, der den Forschern bislang Rätsel aufgab. Die wegweisende Forschungsleistung wurde von der EU teilfinanziert und im Fachblatt Cell veröffentlicht. Das Forscherteam enthüllte, wie eine Hefezelle mithilfe eines fließbandähnlichen Mechanismus beschädigte Proteine in die Mutterzelle zurückführt, bevor aus ihr eine neue Tochterzelle hervorgeht - dieser Prozess wird auch als Mitose bezeichnet. "Auf diese Weise übernimmt die Tochterzelle keine altersbedingten Schäden", sagte Professor Thomas Nyström vom Zell- und Molekularbiologischen Institut der Universität Göteborg, Schweden. Das Forscherteam um Professor Nyström hatte bereits mehrere Studien über Zellalterung veröffentlicht, die neue Entdeckung jedoch ist das Kernstück des Puzzles. Die Studie wurde im Rahmen der EU-finanzierten Projekte MIMAGE (Role of mitochondria in conserved mechanisms of ageing) mit 7,4 Millionen EUR und PROTEOMAGE (Functional analysis of evolutionarily conserved mechanisms of ageing on advanced proteome analysis) mit 10,7 Millionen EUR unter dem Themenbereich "Biowissenschaften, Genomik und Biotechnologie im Dienste der Gesundheit" des Sechsten Rahmenprogramms (RP6) finanziert. Die Studie zeigt, wie Tochterzellen mittels fließbandartiger Strukturen beschädigte Proteine zurück zur Mutterzelle transportieren, um jung und gesund ins Leben zu starten. "Man war immer davon ausgegangen, dass diese Strukturen nur in eine Richtung funktionieren, und zwar indem Proteine und Organellen von der Mutter- zur Tochterzelle wandern", erklärte Professor Nyström. "Nun haben wir nachgewiesen, dass beschädigte Proteine auch in die andere Richtung transportiert werden. Genau genommen nutzt die Tochterzelle die Mutterzelle als Mülleimer, um alle Überreste aus Alterungsprozessen abzuladen, sodass die neu entstandene Zelle keine altersbedingten Schäden übernehmen muss." Die Forscher entdeckten, dass der Transport auf mechanischem Weg über Filamente (Stränge) aus Aktin realisiert wird, die nach dem Fließbandprinzip arbeiten. Zur Herstellung von Aktinfilamenten wird das Gen SIR2 benötigt. Dass Veränderungen am SIR2-Gen die Lebenszeit einer Zelle deutlich verlängern können, hatten bereits frühere Studien gezeigt. "Eine erhöhte SIR2-Aktivität steht für ein längeres Leben, Schädigungen dieses Gens hingegen beschleunigen den Alterungsprozess", erklärte Professor Nyström. "Das wurde bereits an Hefen, Würmern, Fliegen und Fischen nachgewiesen und demnächst vielleicht auch an Säugerzellen." Nach Meinung Professor Nyströms könnten die neuen Erkenntnisse über den Rücktransport geschädigter Zellbestandteile zur Mutterzelle neue Wege eröffnen, um beim Menschen altersbedingte Erkrankungen durch Proteintoxizität zu behandeln, obwohl die genaue Vorgehensweise hierfür noch unklar ist. "Zuerst muss untersucht werden, ob der Transport geschädigter Proteine auch in Säugetieren oder sogar Menschen stattfindet, beispielsweise bei der Entstehung von Keimzellen oder Stammzellen", so der Professor. An den EU-finanzierten Projekten MIMAGE und PROTEOMAGE beteiligten sich insgesamt 31 Partner aus 12 EU-Mitgliedstaaten einschließlich Kanada und China.
Länder
Schweden