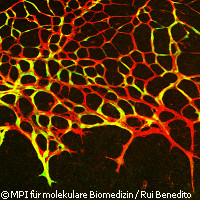
Descubren un interruptor regulador del crecimiento de los vasos sanguíneos
Científicos europeos han identificado un «interruptor» que regula el crecimiento de los vasos sanguíneos. Los descubrimientos, publicados en la revista Cell, podrían ser útiles para el desarrollo de tratamientos contra enfermedades y afecciones caracterizadas por un crecimiento excesivo o insuficiente de vasos sanguíneos. Durante los procesos de desarrollo, crecimiento y curación, se forman nuevos vasos sanguíneos que dan lugar a una compleja red que se extiende hasta donde sea necesario para que todos los tejidos reciban un aporte continuo de oxígeno y nutrientes. Cuando este proceso falla, los resultados pueden ser fatales, produciéndose por ejemplo un infarto si se detiene el riego sanguíneo a los tejidos cardíacos. En este caso, la comunidad científica querría averiguar la forma de promover el crecimiento de nuevos vasos sanguíneos en el corazón. Por otro lado, los tumores cancerosos se mantienen con vida gracias a una red de vasos sanguíneos, razón por la cual sería de gran utilidad el poder bloquear el crecimiento de nuevos vasos sanguíneos y así ahogar al tumor. Hace mucho tiempo que se viene buscando el mecanismo que determina cuándo un vaso sanguíneo debe ramificarse en dos y cuándo no. En este último estudio, científicos de Alemania y Reino Unido identificaron un interruptor que controla el destino de células individuales. En dicho interruptor se encuentra la proteína «Notch», la cual se encuentra en la superficie de las células que recubren las paredes de los vasos sanguíneos. Dependerá de qué proteína sea la que se adhiera a una Notch para que ésta se active o desactive. Si se activa, la célula se vuelve sensible a una molécula denominada factor de crecimiento endotelial vascular (VEGF). Tal y como su nombre indica, la VEGF induce el crecimiento de nuevos vasos sanguíneos. En este estudio, los investigadores descubrieron que la proteína «Jagged1» activa la proteína Notch y provoca que se formen nuevos vasos sanguíneos. Jagged1 se sitúa en la superficie de las células y es capaz de adherirse a los interruptores Notch de las células vecinas. «Ahora comprendemos cómo funcionan todos estos componentes cuando trabajan al unísono», comentó el profesor Ralf Adams del Instituto Max Planck de Biomedicina Molecular (Alemania). «Mediante experimentos realizados con ratones pretendemos aprender a controlar de forma activa el crecimiento de los vasos sanguíneos.» Llegará un día en el que existirán fármacos para hacer lo mismo en humanos, aventuró. Hoy en día ya se puede tratar algunos cánceres y enfermedades oculares mediante el bloqueo de la actividad de VEFG. No obstante, los tratamientos son caros y sus efectos secundarios hacen que sean desaconsejables para muchos pacientes. «Al esclarecer la función de la Jagged1 esperamos haber descubierto una alternativa válida para aplicar tratamientos en un futuro» afirmó el Dr. Rui Benedito, también perteneciente al Instituto Max Planck de Biomedicina Molecular. El siguiente paso para los investigadores consiste en realizar una investigación concienzuda acerca de la efectividad de tratamientos que actúen sobre las proteínas Notch y también acerca de si conllevan o no efectos secundarios peligrosos. Este punto es importante puesto que las Notch desempeñan funciones destacadas en el desarrollo de los sistemas nervioso e inmunológico, por citar dos ejemplos. «Noth, Dll4 [una proteína de la que se sabe que ralentiza la creación de nuevos vasos sanguíneos] y Jagged1 también desempeñan funciones importantes en otros órganos y tipos de células» explicaron el profesor Adams y el Dr. Benedito. «Por eso constituye todo un reto el hecho de limitar los efectos [de un fármaco] únicamente a los vasos sanguíneos. Pese a todo, confiamos en que nuestro trabajo conducirá al desarrollo de nuevos medicamentos.»
Países
Alemania, Reino Unido