Première plateforme d’ingénierie permettant de modéliser l’axe microbiote-intestin-cerveau
Malgré la prévalence et les coûts socio-économiques des maladies neurodégénératives comme la maladie d’Alzheimer, leurs déclencheurs demeurent entourés d’un épais mystère. Le lien entre le cerveau, l’intestin et sa microflore intestinale pourrait constituer une source potentielle. Proposé pour la première fois il y a un siècle, ce domaine de recherche laisse entendre que certaines maladies neurodégénératives sont influencées par le régime alimentaire et le mode de vie. «Nous avons maintenant la preuve que le vieillissement, les régimes alimentaires malsains et le stress ont une influence sur le microbiote intestinal; de plus en plus de données indiquent que ces phénomènes ont une incidence sur les fonctions cérébrales. Nous manquons toutefois d’outils de recherche in vitro pour passer d’une corrélation à un lien de causalité», explique Carmen Giordano, coordinatrice du projet MINERVA, financé par le Conseil européen de la recherche (CER). MINERVA a mis au point la première plateforme d’ingénierie multi-organes, qui permet de modéliser les liens biologiques clés le long de l’axe microbiote-intestin-cerveau. «Il s’agit d’une réalisation exceptionnelle pour l’étude des mécanismes biochimiques qui sous-tendent l’hypothèse microbiote-neurodégénérescence et pour la recherche de traitements fondés sur le régime alimentaire», ajoute Carmen Giordano, professeure associée à l’université polytechnique de Milan, hôte du projet.
Une plateforme multi-organes révolutionnaire
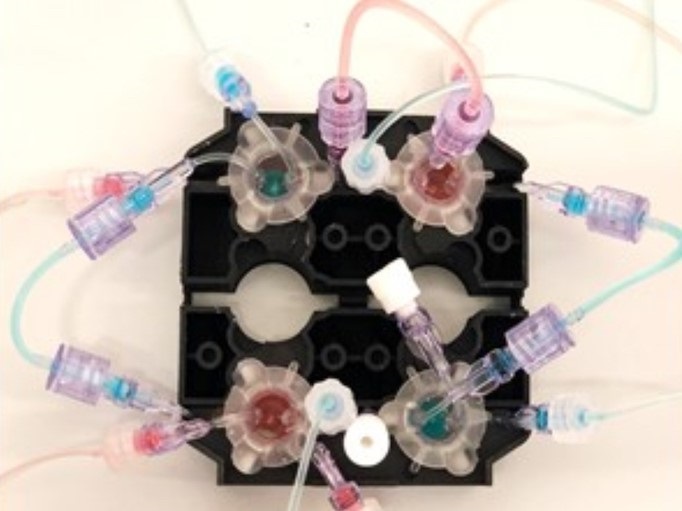
La plateforme multi-organes de MINERVA comporte trois compartiments interconnectés. Chacun d’eux accueille des dispositifs brevetés d’organes sur puce millifluidiques chargés de modèles cellulaires représentant les caractéristiques clés du cerveau et de la barrière hémato-encéphalique, de l’épithélium intestinal et du système immunitaire, et du microbiote. Ces dispositifs sont reliés les uns aux autres de manière hydraulique afin de simuler le transport le long de l’axe de molécules bioactives, principalement le sécrétome, produit par le microbiote. Les modèles cellulaires in vitro au sein de ces dispositifs ont été élaborés dans le but de simuler les caractéristiques clés des systèmes biologiques pertinents. Par exemple, le compartiment microbiote est capable de cultiver des bactéries dans une matrice de polymères 3D modélisant le mucus intestinal, un composant essentiel de l’épithélium intestinal. Tandis que dans le compartiment cerveau, un nouveau modèle de cellules cérébrales en 3D simule le tissu cérébral et d’autres caractéristiques biologiques, dans des conditions physiologiques et pathologiques normales.
Validation de la plateforme
La plateforme représentait à la fois des conditions saines et des conditions neurodégénératives. Deux conditions de culture ont été mises en place dans le compartiment cerveau. Les neurones, les astrocytes et la microglie, à savoir les principales cellules du cerveau, ont été co-cultivés afin d’étudier les effets du microbiote, et cultivés individuellement en vue d’examiner l’incidence du microbiote sur chaque type de cellule. L’équipe a cultivé un microbiote intestinal humain connu pour endommager les cellules cérébrales en activant le système neuro-immunitaire, ainsi qu’un microbiote intestinal complet prélevé chez des patients souffrant de la maladie d’Alzheimer et chez des donneurs sains, après son interaction avec le mucus intestinal. Le sécrétome ainsi produit a ensuite circulé dans la plateforme chargée de cellules; la réponse des cellules cérébrales a ensuite été évaluée. «La comparaison de scénarios sains et neurodégénératifs nous a permis de constater la même réponse des cellules cérébrales à des stimuli préjudiciables du microbiote, telle que documentée dans la littérature et vécue par les patients. Cet exercice confirme que notre approche et notre outil de bioingénierie sont capables de révéler les déclencheurs microbiote-cerveau», explique Carmen Giordano.
L’avenir de la modélisation des maladies
MINERVA contribue au domaine naissant de la modélisation des maladies et ouvre également la voie à un nouveau domaine combinant la bio-ingénierie et les neurosciences qui permettrait d’explorer d’autres pathologies/troubles, notamment l’autisme, la sclérose en plaques et les maladies auto-immunes. En outre, le projet permettrait de modéliser l’incidence des antibiotiques ou d’autres médicaments sur l’organisme. Élément encore plus crucial, étant donné que le microbiote humain peut être modifié par le régime alimentaire, ces travaux ont d’importantes implications thérapeutiques. En introduisant des prébiotiques (ingrédients alimentaires) et des probiotiques (souches de bactéries aux effets bénéfiques sur la santé) sélectionnés, la plateforme pourrait contribuer à l’identification des changements alimentaires et de mode de vie appropriés, ce qui permettrait d’élaborer des stratégies thérapeutiques et préventives non invasives et efficaces. «La polyvalence de notre modèle expérimental permet aux chercheurs d’étudier les mécanismes cellulaires et moléculaires qui sous-tendent, potentiellement, toutes les maladies multi-organes graves», précise Carmen Giordano. En plus d’avoir promu les travaux de MINERVA à de nombreuses occasions, Carmen Giordano a obtenu une subvention CER «Preuve de concept» en 2019 pour le projet DIANA, axé sur le criblage de médicaments ciblant le cerveau. Elle a également bénéficié d’un financement pour le projet MIUR-FARE PEGASO (du ministère de l’université et de la recherche d’Italie), qui teste actuellement la plateforme MINERVA à des fins de médecine personnalisée.
Mots‑clés
MINERVA, microbiote, intestin, cerveau, Alzheimer, neurodégénérative, régime alimentaire, neurones, bactéries, organe sur puce