La questione inaspettatamente complessa dell’accumulo e della perdita di grasso
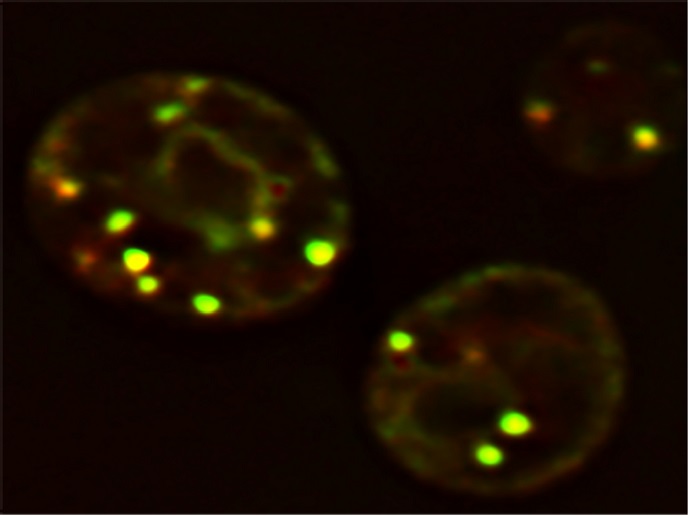
Comprendere la formazione delle LD è fondamentale per scoprire la fisiopatologia dell’obesità e delle malattie associate, come il diabete di tipo 2, l’aterosclerosi e la malattia del fegato grasso. La biogenesi delle LD si verifica nel labirinto delle membrane nel citoplasma, noto come reticolo endoplasmatico. Vedere le LD gialle brillanti in cellule di lievito nell’illustrazione in alto. Tuttavia, ciò che determina nel reticolo endoplasmatico i siti di biogenesi delle LD resta un mistero. Supportato dal programma Marie Skłodowska-Curie, «l’obiettivo principale del progetto LD_Biogenesis era identificare e caratterizzare i siti di biogenesi delle LD nel reticolo endoplasmatico», spiega il borsista Vineet Choudhary.
Le proteine collaborano con fattori di biogenesi
I risultati della ricerca hanno dimostrato che le LD non si formano spontaneamente in posizioni casuali all’interno del reticolo endoplasmatico, ma hanno origine in siti distinti predefiniti dello stesso, contrassegnati dalla proteina seipina, i quali collaborano con diversi fattori di biogenesi LD per stabilire la formazione di goccioline. Ciò che è interessante è che la seipina è una proteina non enzimatica coinvolta nelle sindromi di lipodistrofia, un gruppo di disturbi caratterizzati dalla perdita selettiva di tessuto adiposo. «La proteina seipina svolge un ruolo decisivo nell’avvio della biogenesi delle LD, la cui mancanza si traduce nella nascita di LD in siti ectopici», afferma Choudhary. I risultati della ricerca sono stati pubblicati sulla rivista Journal of Cell Biology. I ricercatori hanno utilizzato lievito di birra, Saccharomyces cerevisiae, appositamente progettato per dimostrare dove sono assemblate le LD nel reticolo endoplasmatico, e una nuova sonda che si illumina quando rileva un sito in cui si accumula il triacilglicerolo (TG). Grazie alla fluorescenza e alla microscopia elettronica, i ricercatori hanno mappato i sottodomini pertinenti. Effettuando knock-out genetici di fattori di biogenesi LD, i ricercatori hanno dimostrato che la seipina insieme alla proteina Nem1 sono necessarie per costruire siti di biogenesi LD funzionali. I siti Seipina-Nem1 vengono associati ad altri fattori di biogenesi delle LD, tra cui Pex30, una proteina che modella la membrana, per agevolare la nascita e la crescita delle LD. Choudhary spiega ulteriormente il ruolo potenziale della seipina: «Abbiamo dimostrato che se la seipina è assente, il TG viene sintetizzato in posizioni casuali nel reticolo endoplasmatico, con conseguente assemblaggio di LD inadeguate in posti sbagliati». Il modo in cui questa biogenesi irregolare delle LD si manifesta nella lipodistrofia è una domanda interessante per ulteriori ricerche.
Sfide e alcuni risultati a sorpresa
«Abbiamo dovuto ottimizzare diversi parametri per far funzionare la tecnica per la luce correlativa e la microscopia elettronica», spiega Choudhary. «Allo stesso modo, abbiamo dovuto ottimizzare l’espressione e la purificazione di una quantità sufficiente di TG sintasi, sLro1, per eseguire test di legame lipidico in vitro». Uno dei risultati sconcertanti di questo studio è la localizzazione sia della seipina che delle proteineNem1 in siti distinti del reticolo endoplasmatico, anche in assenza di LD. Sarà interessante sapere cosa guida la loro co-localizzazione in questi sottodomini di reticolo endoplasmatico. «Resta da determinare se sia mediata da segnali proteici o lipidici, oppure da una combinazione di entrambi. Sapere di più su come si formano questi sottodomini di reticolo endoplasmatico aprirà la strada per decifrare il meccanismo della biogenesi delle LD», afferma Choudhary, con entusiasmo, riferendosi ai suoi piani per la ricerca futura.
Parole chiave
LD_Biogenesis, LD, seipina, obesità, gocciolina lipidica, reticolo endoplasmatico