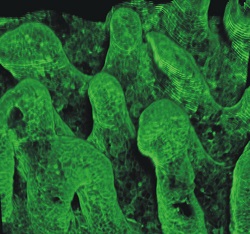
Inżynieria tkankowa łagodzi skutki chorób i zaburzeń układu pokarmowego
Funkcjonalne modele tkanek nabłonkowych in vitro są kluczowymi elementami w podstawowych badaniach biologicznych, modelowaniu chorób, odkrywaniu leków oraz medycynie regeneracyjnej i spersonalizowanej. Kliniczne zastosowania inżynierii tkankowej są utrudnione ze względu na ryzyko zakażenia bakteryjnego z powodu braku funkcjonalnych tkanek inżynierii nabłonkowej. W przypadku nabłonka jelita cienkiego potrzebne są funkcjonalne modele in vitro, aby dokładnie przewidzieć wchłanianie leków podawanych doustnie. Bezproblemowe strategie mikrowytwarzania „Ostatecznym celem projektu COMIET jest opracowanie modeli tkanki nabłonkowej jelita, które naśladują cechy fizjologiczne występujące w tkankach jelitowych człowieka in vivo”, mówi prof. Elena Martinez, kierownik projektu ERBN. Aby to osiągnąć, podejście eksperymentalne połączy techniki mikrowytwarzania, elementy inżynierii tkankowej oraz właściwości organoidów jelitowych dotyczące samoorganizowania się. Do tej pory zespół opracował prostą strategię mikrofabrykacji struktur typu villi 3D na bardzo miękkich materiałach. Model 3D wykazuje parametry funkcjonalne, które są bardziej zbliżone do tkanki fizjologicznej niż konwencjonalne płaskie monowarstwowe systemy hodowli. Poprawi to na przykład przewidywalność wchłaniania leków. Ustalenia te zostały złożone do publikacji i stanowią podstawę do pracy doktorskiej. Według prof. Martinez, badacze opracowali strategię „otwierania” organoidów jelitowych, które są trójwymiarowymi strukturami zamkniętymi. Celem jest formowanie monowarstw, które pokrywają płaskie podłoża i opracowane w projekcie rusztowania 3D. Wyniki zostały przedstawione na sympozjum Organoids EMBO I EMBL w 2016 roku i wkrótce zostaną opublikowane. Partnerzy projektu wykazali również, że architektura 3D typu villi ma bezpośredni wpływ na adhezję bakterii i potencjał inwazyjności. Modele ludzkiego jelita in vitro, które wiernie odtwarzają zachowanie in vivo Prof. Martinez wyjaśnia, że najważniejszym rezultatem projektu COMIET będzie wykazanie, że strategie inżynierskie mogą być z powodzeniem stosowane w celu zapewnienia komórkom macierzystym nabłonka jelita fizycznych i biochemicznych informacji, które kierują ich kompartmentalizacją, tworzeniem barier i odnową tak jak in vivo. „Jeśli koncepcja ta zostanie z powodzeniem zademonstrowana, podobne podejście można będzie zastosować do naśladowania innych tkanek nabłonkowych o złożonej geometrii, takich jak nerki, skóra czy płuca”, mówi badaczka. W dziedzinie badań podstawowych użytkownicy końcowi skorzystają dzięki systemowi łączącemu najważniejsze cechy fizjologiczne tkanki in vivo. W rezultacie może być stosowany w badaniach rozwojowych, ale także jako model chorób człowieka in vitro. Uczeni zaangażowani w badania przesiewowe leków, badania wchłanianie leków i testy toksykologiczne również odniosą korzyści z systemu, który poprawia przewidywalność obecnych testów. „Celem projektu COMIET jest otwarcie nowych ścieżek badań w zakresie chorób jelit”, podsumowuje prof. Martinez. „Na powstaniu systemu skorzystają ostatecznie pacjenci, ponieważ system może być wykorzystany w zindywidualizowanych strategiach medycznych”.
Słowa kluczowe
COMIET, tkanki nabłonkowe, modelowanie in vitro, mikrowytwarzanie, inżynieria tkankowa