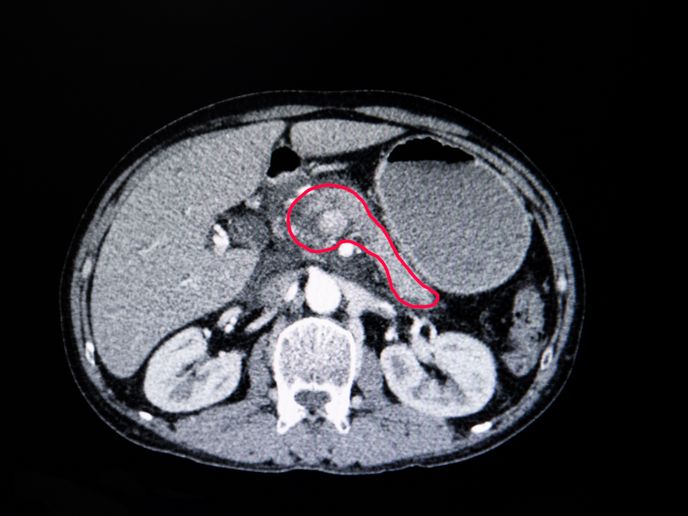
Una primicia para el tratamiento del cáncer de páncreas en modelos murinos
A pesar de ser una de las principales causas de muerte en todo el mundo, la mayoría de los cánceres responden al tratamiento si se detectan a tiempo. Los cánceres de páncreas y pulmón, sin embargo, destacan por sus bajas tasas de supervivencia. «Estos cánceres no suelen presentar síntomas hasta que están muy avanzados, lo que dificulta sobremanera la extirpación quirúrgica del tumor u otros tratamientos», afirma Mariano Barbacid, coordinador del proyecto THERACAN, financiado por el Consejo Europeo de Investigación. Dado que ambos tipos de cáncer están provocados por mutaciones genéticas específicas, conocidas como oncogenes KRAS, el equipo de THERACAN utilizó modelos tumorales («in vivo» e «in vitro») de ratones modificados genéticamente (RMG) para investigar los mecanismos moleculares subyacentes responsables. El equipo del proyecto identificó nuevas dianas terapéuticas implicadas en la señalización oncogénica de KRAS al demostrar que las células tumorales retrocedían en ambos cánceres tras eliminar estas dianas mediante manipulación genética.
El papel de los oncogenes KRAS
Según Barbacid, los oncogenes KRAS son responsables de aproximadamente una cuarta parte de todos los tumores humanos sólidos, incluido el 25 % de los adenocarcinomas (cánceres que se originan en las glándulas que recubren los órganos) y más del 90 % de los tumores pancreáticos. A pesar de ser uno de los primeros oncogenes humanos que se descubrieron (en 1982), hasta hace poco se creía que, debido a su tamaño y forma, las oncoproteínas KRAS no podían ser una diana terapéutica de fármacos. Recientemente las empresas farmacéuticas han sido capaces de diseñar fármacos inhibidores selectivos de los oncogenes KRAS. Sin embargo, como explica Barbacid, las opciones siguen siendo limitadas. «Hasta ahora, la Administración de Alimentos y Medicamentos de los Estados Unidos solo ha aprobado dos fármacos inhibidores para una de las formas mutadas de KRAS. Por desgracia, los resultados clínicos han sido modestos, ya que solo la mitad de los pacientes con cáncer de pulmón experimentan una remisión tumoral. La tasa de supervivencia del cáncer de pulmón a los dos años fue la misma que la observada con los antiguos tratamientos citotóxicos. Los resultados fueron aún menos impresionantes en los tumores de páncreas, por lo que urge desarrollar nuevos inhibidores».
Ratones modificados genéticamente
Los modelos tumorales en RMG permitieron al equipo suprimir las dianas de proteínas oncogénicas sospechosas de desempeñar un papel importante en el desarrollo tumoral. El equipo demostró que la eliminación de RAF1, una proteína implicada en la señalización de KRAS (que controla la proliferación celular, incluida la de los cánceres), provocaba la remisión de dos terceras partes de los tumores de pulmón mutantes de KRAS. Y lo que es aún más importante, la eliminación tanto de RAF1 como del receptor del factor de crecimiento epidérmico (RFCE), que también es parte del proceso de señalización, provocaba la remisión completa de un alto porcentaje de adenocarcinomas ductales pancreáticos. Como no existen inhibidores selectivos de RAF1 que puedan utilizarse para validar los resultados, el equipo lo hizo en modelos tumorales de xenoinjertos derivados de pacientes (células tumorales humanas cultivadas en ratones). Al mismo tiempo, el medicamento contra el cáncer, gefitinib, se utilizó como inhibidor del RFCE. «Este fue el primer informe de la remisión completa de este tipo de tumor en cualquier modelo experimental —señala Barbacid—. Aunque lo demostramos en un modelo animal (y, por tanto, no directamente comparable al humano), observar la desaparición completa de los tumores pancreáticos fue sumamente emocionante».
Acelerar la disponibilidad de nuevos tratamientos
Dado que los tratamientos farmacéuticos suelen tardar muchos años en pasar de los ensayos clínicos a la práctica médica, los proyectos como THERACAN desempeñan un papel vital en la identificación de dianas prometedoras para la intervención terapéutica. «Nuestro trabajo ayuda a la industria farmacéutica a centrar sus recursos y, así, reducir el tiempo que se tarda en desarrollar los fármacos inhibidores selectivos, lo que en última instancia beneficia a los enfermos de cáncer», concluye Barbacid. El equipo está llevando a cabo ahora un proyecto financiado con fondos europeos para desarrollar nuevas estrategias genéticas que hagan remitir por completo todos los tumores de pulmón y páncreas mutantes de KRAS en modelos de RMG.
Palabras clave
THERACAN, cáncer, mutaciones genéticas, pancreático, pulmón, tumores, KRAS, oncogenes, célula, proteína, farmacéutico