Le nanoparticelle distribuiscono farmaci direttamente al cervello
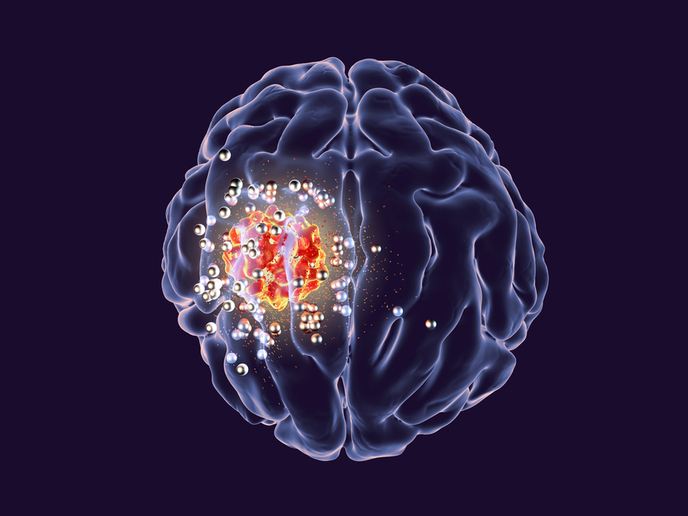
I tumori cerebrali sono difficili da trattare a causa della loro natura invasiva e aggressività. Un altro grande ostacolo è rappresentato dalla protezione naturale del cervello che lo separa dalla circolazione sistemica, rendendo problematico il trattamento con farmaci sistemici.
Un approccio basato su polimeri per la distribuzione dei farmaci
Intrapreso con il supporto del programma Marie Skłodowska-Curie, il progetto HyGlio ha affrontato il tema della distribuzione dei farmaci al cervello e dell’imaging attraverso lo sviluppo di uno strumento multifunzionale basato su polimeri che combina idrogel e nanoparticelle. «Combinando idrogel e nanoparticelle, possiamo unire il vantaggio del rilascio a lungo termine dagli idrogel e la capacità di targeting delle nanoparticelle, nella speranza di prolungare il tempo di permanenza dei farmaci nell’area del tumore», spiega Clara Mattu, borsista Marie Skłodowska-Curie. HyGlio è stata una collaborazione tra il Politecnico di Torino e lo Houston Methodist Research Institute negli Stati Uniti, dove la borsista ha trascorso 2 anni nell’ambito della fase «outgoing» del progetto. Nel progettare particelle per la distribuzione dei farmaci, gli scienziati devono tenere conto delle proprietà superficiali dei vettori di nanoparticelle in quanto essi determineranno l’interazione cellulare, la biodistribuzione in vivo e l’accumulo tumorale. In questo contesto, la borsista ricercatrice ha impiegato nanoparticelle a base di poliuretano con diametro di 100-200 nm per caricare i farmaci. Queste nanoparticelle contenevano domini sia idrofobi che idrofili che miglioravano l’affinità per i farmaci sia idrofili che idrofobi e mostravano un miglioramento complessivo della biodistribuzione e dell’emivita all’interno del corpo. La borsista ha inoltre combinato nanoparticelle con idrogel che sono adatti per la distribuzione localizzata di farmaci e agevolano il rilascio lento. L’uso di idrogel termo-reattivi ha garantito che il gel fosse liquido e iniettabile a temperatura ambiente e formasse rapidamente una rete 3D al raggiungimento della temperatura corporea nel luogo di iniezione. Per studiare il tumore, ha caricato le nanoparticelle con marcatori fluorescenti o altre sonde di imaging che consentono la risonanza magnetica per immagini. «Noi, come altri, abbiamo dimostrato che è possibile ottenere il caricamento concomitante di farmaci e sonde di imaging all’interno di nanoparticelle», sottolinea.
Efficacia del metodo di distribuzione dei farmaci in idrogel
Sebbene il metodo sia nelle prime fasi dello sviluppo, i dati preliminari in vivo suggeriscono che la combinazione di idrogel e nanoparticelle sia sicura e, soprattutto, che le nanoparticelle possano risiedere nel cervello e in prossimità del tumore più a lungo. Gli animali sperimentali portatori di tumore hanno trattenuto nanoparticelle caricate con farmaci fino a 10 giorni dopo l’iniezione intra-tumorale e il farmaco ha mostrato una buona biodistribuzione nel tumore, migliorando la sopravvivenza degli animali. Gli scienziati hanno inoltre osservato modifiche nel numero e nella struttura dei vasi sanguigni tumorali dopo il trattamento. I piani futuri includono test di combinazioni di farmaci in strategie a doppio rilascio, dove i farmaci vengono caricati in parte in nanoparticelle e in parte nel compartimento dell’idrogel. La terapia del cancro spesso richiede l’azione concertata e combinata di diversi chemioterapici per superare la resistenza ai farmaci e migliorare l’esito del paziente. Tuttavia, il trattamento sinergico è ostacolato da una farmacocinetica incompatibile e dall’idrofobicità dei diversi farmaci. HyGlio propone di ovviare a questo attraverso la combinazione di idrogel con nanoparticelle in poliuretano per un efficace incapsulamento di farmaci sia idrofobi che idrofili, ottenendo il massimo accumulo tumorale e la massima efficacia del trattamento.
Parole chiave
HyGlio, farmaco, nanoparticella, idrogel, distribuzione dei farmaci, biodistribuzione, tumore cerebrale, poliuretano