Heterogeniczność genomu białaczki: podwaliny pod terapię celowaną
Ostra białaczka limfoblastyczna (OBL) to najczęściej występująca u dzieci choroba nowotworowa, Powstaje ona w krwiotwórczych komórkach macierzystych, które w wyniku nagromadzenia mutacji genetycznych przekształcają się w złośliwe białe krwinki. Komórki OBL nie są genetycznie podobne, a podczas diagnozy rozpoznawanych jest od 10 do 20 ważnych mutacji genetycznych. Trwają poszukiwania odpowiedzi na pytanie dotyczące sposobu, w jaki konkretna kombinacja mutacji przekształca normalne komórki w szybko rozwijające się komórki białaczki.
Mutacje w komórkach OBL
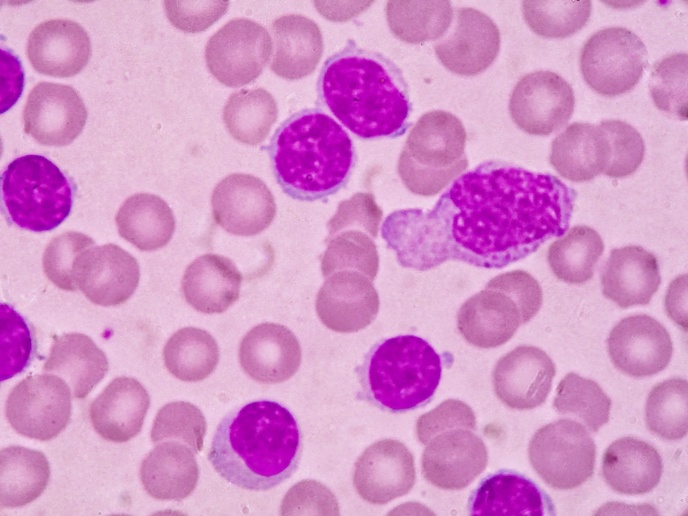
Głównym celem zespołu projektu scTALLmap było zbadanie heterogenności wewnątrz guza, czyli obecności różnych klonów genetycznych komórek OBL w momencie diagnozy. Badania zostały przeprowadzone dzięki wsparciu z programu działań „Maria Skłodowska-Curie” i z wykorzystaniem technologii jednokomórkowych, które umożliwiają analizę genomu ponad osiem tysięcy pojedynczych komórek w ramach jednego badania. „Chociaż wszystkie komórki pacjentów z białaczką pod mikroskopem wyglądają tak samo, odkryliśmy, że w rzeczywistości się różnią”, wyjaśnia Jan Cools, profesor genetyki człowieka na Katolickim Uniwersytecie Lowańskim (KU Leuven) i Flandryjskim Instytucie Biotechnologii będącym gospodarzem projektu. Zazwyczaj 1–10 % komórek OBL ma inne mutacje niż reszta nowotworu, co świadczy o tym, że proces rozwoju białaczki nie jest liniowy, a w komórkach po prostu wykształca się coraz więcej mutacji. Proces ten trwa prawdopodobnie od kilku miesięcy do kilku lat, a kiedy komórki uzyskają odpowiednią kombinację mutacji, przekształcają się w szybko postępującą białaczkę, która eliminuje zdrowe komórki w szpiku kostnym, krwi i innych narządach krwiotwórczych.
Analiza mutacji komórek OBL na poziomie pojedynczej komórki
Zespół projektu scTALLmap zbadał genom pojedynczych komórek i odkrył obecność różnych mutacji w obrębie tego samego genu. Oznacza to, że kilka komórek może niezależnie od siebie nabyć mutację w tym genie, co podkreśla jego znaczenie w rozwoju białaczki. Ponadto często kilka mutacji wykształca się w tej samej ścieżce sygnalizacyjnej, więc jedna mutacja wystarczy do pełnej aktywacji tej ścieżki. Uwypukla to także rolę tego szlaku w postępie białaczki. Zespół projektu scTALLmap w szczególności badał sygnalizację NOTCH1 odgrywającą kluczową rolę w rozwoju limfocytów T i wyborze linii komórkowej. Naukowcy ustalili, że pacjenci zazwyczaj mają więcej niż jedną mutację NOTCH1, różne komórki mogą mieć różne mutacje NOTCH1 i że mutacje te są jednymi z ostatnich mutacji w komórkach białaczki.
Przyszłość klonalnej analizy OBL
Zdaniem Cools, „najważniejszym osiągnięciem projektu było szczegółowe zmapowanie wszystkich możliwych mutacji w obrębie pojedynczych komórek białaczki”, co może pomóc w opisaniu początków białaczki i rozpoznaniu wywołujących ja mutacji. Ponadto ustalenia te dostarczają wiedzy na temat ewolucji białaczki i czasu powstawania mutacji. Zrozumienie heterogeniczności tej choroby nowotworowej pozwoli na dalszą poprawę skuteczności leczenia i opracowanie terapii celowanych. Chemioterapia zabija wszystkie szybko rosnące komórki, w efekcie wywołując wiele skutków ubocznych. Z kolei terapia celowana działa tylko na komórki nowotworowe mające konkretne mutacje i jest mniej toksyczna dla zdrowych komórek. Duża heterogeniczność białaczki sprawia jednak, że ta metoda leczenia nie zwalcza wszystkich komórek nowotworowych. Wiedza na temat heterogeniczności białaczki pomagać będzie więc w doborze odpowiedniej terapii celowanej.
Słowa kluczowe
scTALLmap, mutacja, OBL, heterogeniczność, terapia celowana, NOTCH1, ostra białaczka limfoblastyczna