Un médicament de fertilité prometteur dans la lutte contre la résistance aux antibiotiques
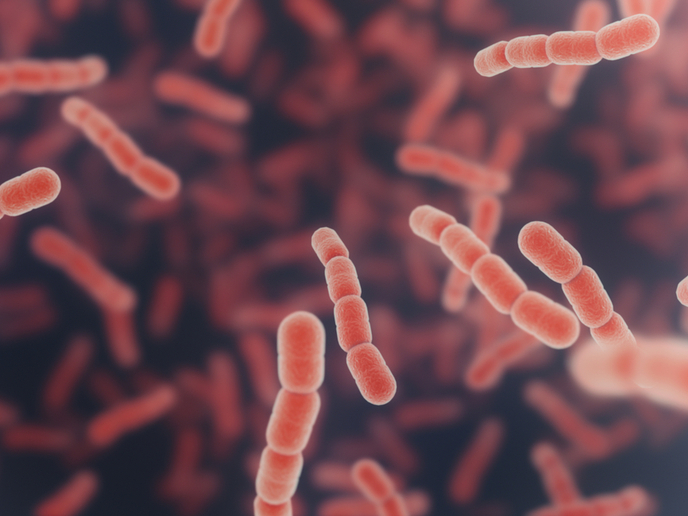
Malgré les efforts considérables déployés pour combattre la bactérie Streptococcus pneumoniae, cet agent pathogène reste une menace grave pour la santé humaine, en particulier chez les jeunes enfants. Chaque année, 14 millions d’enfants âgés de moins de cinq ans souffrent d’une maladie grave à la suite d’une infection, et plus de 800 000 enfants trouvent la mort. Bien que S. pneumoniae puisse être traité avec des médicaments à base de pénicilline comme l’amoxicilline, les souches résistantes sont de plus en plus fréquentes. Le projet GetToKnowPneumo a reçu un financement dans le cadre du programme Actions Marie Skłodowska-Curie pour obtenir de nouvelles informations sur la biologie cellulaire de cette bactérie. Liselot Dewachter, chercheuse à l’université de Lausanne en Suisse, décrit les aspirations du projet: «Outre obtenir des informations détaillées sur le cycle cellulaire, nous espérons être capables de traduire nos résultats en applications pratiques pouvant servir dans la pratique clinique.»
L’importance de la forme
Sachant qu’il peut falloir plus de dix ans pour développer de nouveaux antibiotiques, les chercheurs ont cherché à identifier des médicaments susceptibles de renforcer l’activité antimicrobienne des antibiotiques existants. La combinaison de deux médicaments qui ciblent le même processus peut créer un effet synergétique, la combinaison étant plus efficace que la somme des composés individuels. Comme l’amoxicilline agit en perturbant la croissance et la division des cellules bactériennes, l’équipe a utilisé l’interférence CRISPR pour identifier les gènes responsables du maintien de la taille correcte des cellules. «L’interférence CRISPR est une version modifiée de la technique CRISPR où l’ADN n’est pas découpé, mais où l’expression des gènes ciblés par le système d’interférence CRISPR est inhibée», explique Liselot Dewachter. Les chercheurs ont ensuite utilisé le tri cellulaire activé par fluorescence pour effectuer un dépistage des cellules individuelles en fonction des caractéristiques d’intérêt — dans ce cas, les modifications de la structure cellulaire. «Cette bactérie a généralement une forme ovale qui ressemble à un ballon de rugby. Toutefois, nous avons découvert qu’elles peuvent adopter une forme de tige très longue lorsque certaines protéines font défaut», indique Liselot Dewachter. Son équipe a montré que ce phénotype était dû à un transport insuffisant des précurseurs de la paroi cellulaire à travers la membrane cellulaire, en raison de l’inhibition de l’undécaprényl‑phosphate (Und‑P), le transporteur lipidique responsable de ce processus.
Ancien médicament, nouvelle utilisation
Grâce à ces informations, l’équipe a identifié le clomifène, un médicament de fertilité, comme candidat pour une thérapie combinée avec l’amoxicilline. Ce médicament, approuvé par la FDA, est un inhibiteur de la synthèse de l’Und‑P. En laboratoire, un traitement combiné a rendu S. pneumoniae résistante aux médicaments à nouveau sensible à des concentrations cliniquement pertinentes d’amoxicilline. Si ces résultats se vérifient pour les infections humaines, cette approche peut être utilisée pour inverser de manière efficace la résistance et prolonger la durée de vie clinique de notre arsenal antibiotique actuel. Actuellement, un manuscrit est en cours d’élaboration et sera achevé dans les mois à venir. Les résultats du projet ont été présentés lors de la conférence «Bacterial Morphogenesis, Survival and Virulence: Regulation in 4D» qui s’est tenue en 2019, avant la pandémie de COVID-19, en Afrique du Sud. «Même si le financement du projet s’est terminé, nous poursuivons toujours cet axe de recherche jusqu’à son terme», souligne Liselot Dewachter. Actuellement, des essais in vivo sont effectués par des collaborateurs pour tester le potentiel clinique de cette nouvelle stratégie thérapeutique. «En outre, nous explorons la possibilité de déposer un brevet pour, nous espérons, pouvoir transposer nos résultats dans la pratique clinique.»
Mots‑clés
GetToKnowPneumo, bactéries, antibiotiques, résistance, S. pneumoniae, interférence CRISPR