Fruchtbarkeitsmedikament stellt sich im Kampf gegen Antibiotikaresistenzen als vielversprechend heraus
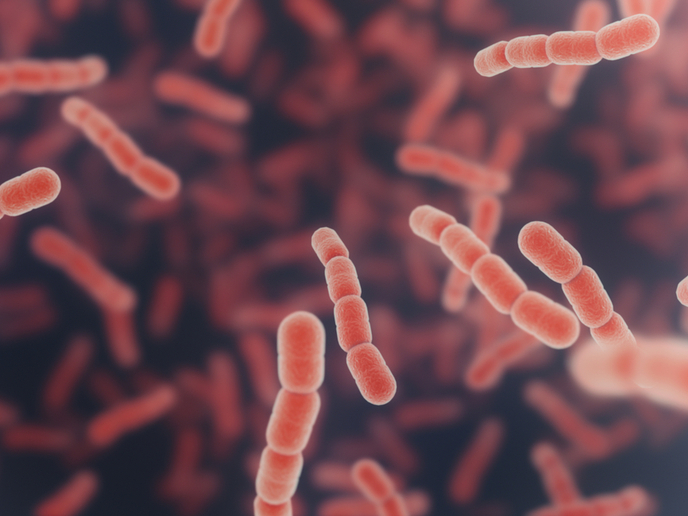
Trotz intensiver Bemühungen im Kampf gegen das Bakterium Streptococcus pneumoniae stellt der Erreger nach wie vor eine ernsthafte Bedrohung für die menschliche Gesundheit dar, insbesondere bei Kleinkindern. Jedes Jahr erkranken 14 Millionen Kinder unter 5 Jahren schwer an einer Infektion, und mehr als 800 000 Kinder sterben daran. Obwohl S. pneumoniae mit Medikamenten auf Penicillinbasis wie Amoxicillin behandelt werden kann, treten immer häufiger resistente Stämme auf. Das über die Marie-Skłodowska-Curie-Maßnahmen finanzierte Projekt GetToKnowPneumo soll neue Erkenntnisse zur Zellbiologie des Bakteriums liefern. Stipendiatin Liselot Dewachter von der Universität Lausanne, Schweiz, erläutert die Projektziele: „Wir wollten nicht nur den Zellzyklus im Detail erforschen, sondern unsere Ergebnisse auch in praktische klinische Anwendungen überführen.“
Die Form ist alles
Da die Entwicklung neuer Antibiotika mehr als ein Jahrzehnt dauern kann, suchten die Forschenden nach Medikamenten, die die antimikrobielle Wirkung vorhandener Antibiotika verstärken könnten. Durch die Kombination von zwei Wirkstoffen, die auf den gleichen Prozess abzielen, können Synergieeffekte entstehen, deren Wirkung stärker ist als die Summe der einzelnen Verbindungen. Da Amoxicillin das Wachstum und die Teilung von Bakterienzellen stört, nutzte das Team CRISPR-Interferenz, um Gene zu ermitteln, die für die Aufrechterhaltung der richtigen Zellgröße verantwortlich sind. „CRISPRi ist eine Weiterentwicklung von CRISPR. Das Prinzip dabei ist nicht das Schneiden von DNA, sondern die Hemmung der Expression von Genen, auf die das CRISPR-Interferenzsystem abzielt“, erklärt Dewachter. Die Forschenden setzten dann die fluoreszenzaktivierte Zellsortierung ein, um einzelne Zellen auf interessante Merkmale zu untersuchen – in diesem Fall auf Veränderungen der Zellstruktur. „Die Form des Bakteriums ist normalerweise oval, ähnlich wie bei einem Rugbyball. Kommt es jedoch zu einer Depletion spezifischer Proteine, kann das Bakterium auch eine deutlich verlängerte Stäbchenform annehmen“, sagt Dewachter. Ihr Team zeigte auf, dass dieser Phänotyp durch einen unzureichenden Transport von Zellwandvorläufern durch die Zellmembran verursacht wird, der auf eine Hemmung von Undecaprenylphosphat (Und-P), dem für diesen Prozess verantwortlichen Lipidträger, zurückzuführen ist.
Altes Medikament, neues Einsatzgebiet
Mit diesen Informationen erfasste das Team das Fruchtbarkeitsmedikament Clomifen als einen Kandidaten für eine Kombinationstherapie mit Amoxicillin. Das von der FDA zugelassene Medikament ist ein Hemmstoff der Und-P-Synthese. Im Labor bewirkte eine kombinierte Behandlung, dass arzneimittelresistente S. pneumoniae wieder empfindlich gegenüber klinisch relevanten Konzentrationen von Amoxicillin wurde. Wenn diese Ergebnisse bei menschlichen Infektionen reproduzierbar sind, wäre dies ein effektiver Ansatz, um die Resistenzbildung umzukehren und die klinische Wirksamkeit herkömmlicher Antibiotika zu verlängern. In den kommenden Monaten wird ein Forschungsbericht zu den Ergebnissen erstellt. 2019, vor Beginn der COVID-19-Pandemie, wurden die Projektergebnisse auf der Konferenz „Bacterial Morphogenesis, Survival and Virulence: Regulation in 4D“ in Südafrika präsentiert. „Auch nach Auslauf der Projektförderung führen wir diese Forschungslinie fort“, sagt Dewachter. Derzeit wird das klinische Potenzial des innovativen Therapieansatzes von Kooperationspartnern in vivo getestet. „Wir prüfen auch Möglichkeiten für einen Patentantrag, um baldmöglichst die klinische Umsetzung zu fördern.“
Schlüsselbegriffe
GetToKnowPneumo, Bakterien, Antibiotika, Resistenz, S. pneumoniae, CRISPRi, CRISPR interference