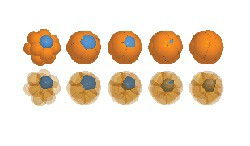
Una simulación cuantitativa del desarrollo embrionario
Las fases iniciales de la embriogénesis se caracterizan por una sucesión estructurada de divisiones, deformaciones y reorganizaciones celulares, a resultas de lo cual se forman dos linajes celulares diferenciados que se separan en una capa interior y otra exterior. La obtención de imágenes precisas en cuatro dimensiones de embriones en sus fases iniciales podría sacar a relucir dinámicas superficiales intensas. El objetivo principal del proyecto MecaMorphEME era crear un modelo físico realista del embrión de ratón antes de su implantación tomando en consideración la interacción entre la contractilidad superficial y la adhesión de célula a célula. El Dr. Hervé Turlier, beneficiario de la subvención, declaró: «En términos más generales, el proyecto tenía el cometido de elaborar un marco numérico que fuese útil para realizar un estudio cuantitativo de la morfogénesis de un grupo reducido de células». Fases cruciales del desarrollo embrionario inicial En la fase de ocho células, el embrión de roedor sufre una compactación cuando los contactos entre las células aumentan de tamaño y el embrión adquiere forma redondeada. Durante la siguiente transición, de la fase de ocho células a la fase de dieciséis células, los blastómeros se separan en dos capas: la masa celular interna (MCI) y la capa epitelial circundante, o trofoectodermo. Los blastómeros se distribuyen espacialmente y, de ese modo, reciben distintos destinos celulares que determinarán su futuro. Las células del trofoectodermo solo forman estructuras extraembrionarias, por ejemplo, la placenta. En cambio, las células de la MCI se transforman en el embrión y en otras estructuras extraembrionarias. El modelo físico de la morfogénesis embrionaria inicial Los investigadores participantes en el proyecto elaboraron un modelo físico mínimo inicial en función de las tensiones superficiales que describe la configuración de los dobletes celulares. Este puede ayudar a entender el proceso de compactación. Para estudiar la formación de la MCI en la transición de ocho a dieciséis células, los investigadores extrapolaron ese enfoque a los dobletes celulares asimétricos. Cada doblete es resultado de una división celular asimétrica que separa un dominio apical formado en la fase de ocho células y lo coloca en una sola de las células hijas. Los datos experimentales muestran que el dominio apical tiene una tensión contráctil reducida. En consecuencia, el doblete tiene forma asimétrica, y esa asimetría conduce a una internalización completa de la célula no apical en su «hermana», que hereda un dominio apical. El marco demuestra que la separación asimétrica del dominio apical genera blastómeros con contractilidad diferente, lo que motiva su separación en las posiciones interna y externa. La modelización tridimensional de la morfogénesis embrionaria permite prever que las células se internalizan cuando las diferencias en la contractilidad superficial superan cierto umbral, y que la forma de los blastómeros del embrión viene determinada por la tensión en su zona de contacto. Conviene destacar que esa previsión pudo validarse experimentalmente y aplicarse para redirigir la separación celular dentro del blastocito en desarrollo dentro del embrión murino. Una aplicación útil del modelo El proyecto MecaMorphEME presentó un marco teórico simple para analizar la mecánica de la internalización celular que conduce a la formación de la MCI en el embrión cuando consta de dieciséis células. Ese es uno de los momentos determinantes en el desarrollo de los embriones de los mamíferos, y el modelo indica que la contractilidad acopla el posicionamiento y la especificación del destino de los blastómeros. En medicina de reproducción asistida, los embriones que se desea implantar se seleccionan antes in vitro mediante inspección visual. Los artífices del proyecto opinan que «los modelos matemáticos pueden ayudar a tomar decisiones más exactas al tener en cuenta la forma de las células del interior del embrión». Tendencias y desarrollos futuros Los integrantes del proyecto han logrado avances apasionantes en la modelización numérica de la morfogénesis embrionaria. Además de aumentar la efectividad de la medicina de reproducción asistida, el profesor François Nédélec y el Dr. Turlier prevén lo siguiente: «Se abren varias opciones que será muy interesante estudiar. Una es acoplar el modelo mecánico con otro modelo de cómo las células responden o transmiten señales a las células adyacentes. Esto es fundamental para desentrañar las complejas dinámicas que tienen lugar en la fase inicial de los embriones de los mamíferos y que conllevan, en concreto, cambios genéticos o epigenéticos».
Palabras clave
MecaMorphEME, contractilidad, MCI, compactación, modelo físico, embriogénesis